NộI Dung
Neulasta (pegfilgrastim) là một loại thuốc được sử dụng để giảm nguy cơ nhiễm trùng ở những người đang điều trị ung thư. Thuốc kích thích sản xuất các tế bào bạch cầu được gọi là bạch cầu trung tính, là cơ quan bảo vệ đầu tiên của cơ thể chống lại vi sinh vật gây bệnh. Neulasta đã được Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) chấp thuận sử dụng cho những người có nguy cơ nhiễm trùng khi đang hóa trị hoặc xạ trị.Làm thế nào nó hoạt động
Một trong những thách thức của hóa trị là các loại thuốc thông thường được sử dụng hoạt động bằng cách nhắm mục tiêu và giết chết các tế bào tái tạo nhanh. Chúng không chỉ bao gồm các tế bào ung thư mà còn các nang tóc, các tế bào của đường tiêu hóa, và cả các tế bào hồng cầu và bạch cầu. Đây là lý do tại sao những người đang hóa trị liệu sẽ thường gặp những hiện tượng như rụng tóc, buồn nôn, nôn và thiếu máu.
Neulasta hoạt động bằng cách kích thích sản xuất bạch cầu trung tính, chiếm tới 60% tế bào bạch cầu và là trung tâm của phản ứng miễn dịch bẩm sinh của bạn.
Pegfilgrastim là dạng pegyl hóa của thuốc filgrastim, một chất tương tự yếu tố kích thích thuộc địa tế bào hạt (G-CSF). Điều này có nghĩa là một chất gọi là polyethylene glycol (PEG) được gắn vào filgrastim để nó tồn tại trong cơ thể lâu hơn trước khi hỏng. Trong thời gian này, tủy xương được kích thích để sản xuất không chỉ bạch cầu hạt như bạch cầu trung tính, mà còn các tế bào bạch cầu khác như basophils và bạch cầu ái toan.
Khi được sử dụng riêng, filgrastim được bán trên thị trường dưới tên thương hiệu Neupogen.
Neulasta so với Neupogen cho hóa trị liệuAi có thể lấy nó
Neulasta được sử dụng để giảm nguy cơ giảm bạch cầu trung tính (số lượng bạch cầu trung tính thấp) ở người lớn hoặc trẻ em đang hóa trị liệu ức chế tủy (ức chế tủy xương). Thuốc này không được dùng cho tất cả mọi người đang hóa trị mà chủ yếu là những người có phác đồ thuốc liên quan đến 17% hoặc cao hơn nguy cơ giảm bạch cầu do sốt (đặc trưng bởi sốt và các dấu hiệu nhiễm trùng khác).
Một nghiên cứu năm 2015 từ Nhật Bản đã báo cáo rằng Neulasta được sử dụng ở phụ nữ bị ung thư vú giai đoạn 4 làm giảm nguy cơ sốt giảm bạch cầu trong quá trình hóa trị liệu 98% so với giả dược.
Các yếu tố khác có thể thúc đẩy việc sử dụng Neulasta, bao gồm:
- Trên 65 tuổi
- Có các tình trạng y tế khác, chẳng hạn như bệnh tiểu đường hoặc bệnh gan, tim hoặc phổi
- Đã từng hóa trị hoặc xạ trị trước đó
- Bị ung thư di căn giai đoạn 4
- Có hệ thống miễn dịch suy yếu
Neulasta cũng có thể được sử dụng cho những người bị ức chế tủy xương nghiêm trọng trong khi điều trị bằng bức xạ (một tình trạng được gọi là hội chứng bức xạ cấp tính, hoặc ARS).
Neulasta là không phải thích hợp cho những người đang điều trị ung thư không tủy. Đây là những loại không liên quan đến tủy máu. Ví dụ bao gồm sarcoma, u ác tính, u lympho, bệnh bạch cầu lymphocytic và đa u tủy.
Liều lượng
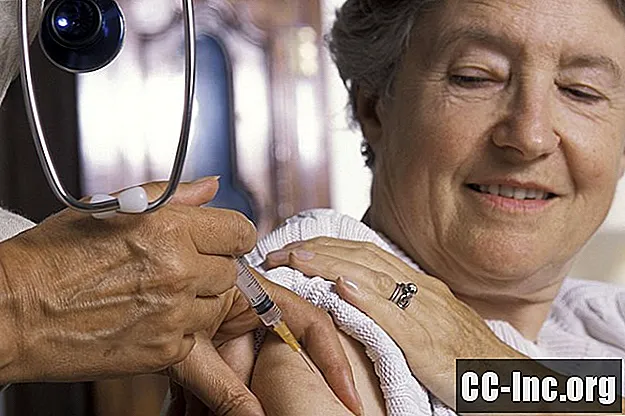
Neulasta được cung cấp bằng cách tiêm trong một ống tiêm chứa sẵn 0,6 mililit (mL). Mỗi ống tiêm chứa 6 miligam (mg) Neulasta. Thuốc được tiêm ngay dưới da ở cánh tay trên, bụng, đùi hoặc mông.
Liều khuyến cáo cho người lớn có thể khác nhau tùy theo loại điều trị như sau:
- Đối với người lớn đang hóa trị, một mũi tiêm 6 mg duy nhất sẽ được tiêm không muộn hơn 24 giờ sau khi truyền xong. Neulasta được tiêm một lần mỗi chu kỳ hóa trị hai hoặc ba tuần.
- Đối với người lớn đang xạ trị, hai mũi tiêm 6 mg, mỗi mũi tiêm cách nhau một tuần, sẽ được bắt đầu ngay khi nhận ra những dấu hiệu đầu tiên của ARS.
Trẻ em được điều chỉnh liều lượng dựa trên cân nặng:
- Dưới 10 kg: 0,1 miligam trên kg trọng lượng (mg / kg)
- 10 đến 20 kg: 1,5 mg
- 21 đến 30 kg: 2,5 mg
- 31 đến 44 kg: 4 mg
- 45 kg trở lên: 6 mg
Liều dùng cũng có thể khác nhau dựa trên sức khỏe hiện tại, tình trạng y tế và loại ung thư bạn mắc phải.
Phản ứng phụ
Như với bất kỳ loại thuốc nào, có thể có tác dụng phụ khi sử dụng Neulasta. Những người trải qua chúng nói chung sẽ có các triệu chứng cấp độ thấp tự hết mà không cần điều trị. Các tác dụng phụ thường gặp nhất ở 26% số người là:
- Đau chỗ tiêm
- Đau xương
Những triệu chứng này có thể được giảm bớt bằng thuốc giảm đau không kê đơn như Tylenol (acetaminophen), Advil (ibuprofen) hoặc Aleve (naproxen). Thuốc kháng histamine Claritin (loratadine) cũng đã được chứng minh là có hiệu quả trong việc giảm đau xương do điều trị.
Các phản ứng dị ứng nghiêm trọng, bao gồm cả phản vệ, không phổ biến nhưng có thể xảy ra. Phần lớn những điều này xảy ra sau lần tiếp xúc ban đầu. Ngay cả khi được điều trị thành công bằng thuốc kháng histamine và các loại thuốc khác, dị ứng do điều trị đã được biết là sẽ tái phát trong những ngày kể từ khi ngừng điều trị chống dị ứng.
Gọi 911 hoặc tìm kiếm sự chăm sóc khẩn cấp nếu bạn phát ban hoặc nổi mề đay, sốt cao, chóng mặt, nhịp tim nhanh hoặc không đều, khó thở, thở khò khè hoặc sưng mặt, lưỡi hoặc cổ họng sau khi nhận Neulasta.
Nếu không được điều trị, sốc phản vệ có thể dẫn đến sốc, hôn mê, suy tim hoặc hô hấp, ngạt thở và tử vong.
Tương tác
Người ta không biết liệu Neulasta có thể gây ra tương tác thuốc hay không. Cho đến nay, vẫn chưa xác định được chính thức. Như đã nói, Neulasta không nên được sử dụng với bất kỳ loại thuốc nào khác có chứa filgrastim do tác dụng phụ. Bao gồm các:
- Neupogen
- Fulphila (pegfilgrastim-jmdb)
- Granix (tbo-filgrastim)
- Nivestym (filgrastim-aafi)
- Udenysa (pegfilgrastim-cbqv)
- Zarxio (filgrastim-sndz)
Chống chỉ định
Chống chỉ định tuyệt đối duy nhất đối với việc sử dụng Neulasta là có tiền sử dị ứng với các chất tương tự G-CSF như Neulasta và Neupogen.
Filgrastim có nguồn gốc từ quá trình lên men của vi khuẩn E. coli. Do đó, bạn cũng có thể cần tránh Neulasta nếu bạn bị dị ứng với E coli-derived asparaginase được sử dụng để điều trị bệnh bạch cầu.
Mặc dù Neulasta không được chống chỉ định trong thời kỳ mang thai, nó nên được sử dụng hết sức thận trọng và chỉ khi lợi ích của việc điều trị lớn hơn nguy cơ có thể xảy ra.
Neulasta được phân loại là thuốc nhóm C cho thai kỳ, có nghĩa là các nghiên cứu trên động vật đã chứng minh khả năng gây hại cho thai nhi nhưng không có nghiên cứu được kiểm soát tốt nào để đánh giá nguy cơ ở người.
Trong số các nghiên cứu trên động vật được thực hiện, tác hại của thai nhi được báo cáo ở liều lượng gấp 4 đến 10 lần đối với người (dựa trên diện tích bề mặt cơ thể). Trọng lượng sơ sinh thấp là biến chứng phổ biến nhất. Các khuyết tật về xương hoặc cơ quan không được báo cáo.
Người ta không biết liệu Neulasta có bài tiết qua sữa mẹ hay không. Các thuốc G-CSF khác được biết là bài tiết kém và hấp thu kém khi uống. Nói chuyện với bác sĩ chuyên khoa ung thư của bạn nếu bạn đang mang thai hoặc dự định có thai để hiểu đầy đủ về những rủi ro và lợi ích của việc điều trị.
Giảm nguy cơ nhiễm trùng trong quá trình hóa trị liệu